Não te esqueças de espreitar o Blog onde terás acesso a mais conteúdos!
(Canto superior direito do menu)
Dia Internacional da Mulher
Irène Joliot- Curie
Para assinalar o Dia Internacional da Mulher, os alunos de Química, no âmbito do projeto Quimiquices 12, prestam homenagem a Irène Joliot-Curie — uma cientista brilhante que marcou a história da ciência e se tornou a segunda mulher a receber o Prémio Nobel da Química.
Neste vídeo, convidamos-te a descobrir a vida, a coragem e o legado de uma mulher que abriu novos caminhos na ciência e inspirou gerações.
Luísa Santos, Cristiana Martins, Diogo Silva, Inês Araújo, João Brandão, Laura Pereira e Rodrigo Trigueiro
9 mar 26

Sabores fabricados:
A Química na comida Fast-Food
Certamente já ouviste dizer — e com razão — que não é aconselhável consumir comida fast-food com muita frequência. Mas porquê? Qual é, afinal, o papel da química neste tipo de alimentação? Serão realmente os conservantes e os aditivos os principais responsáveis pelas preocupações associadas ao seu consumo?
Aqui vais perceber o que compõe este tipo de comida e analisar criticamente o impacto desses componentes na nossa saúde.
A comida fast-food é extremamente industrializada, o que implica a utilização de diversos aditivos químicos. Assim, importa compreender que reações químicas estão associadas a esses compostos e analisar se são, ou não, os verdadeiros responsáveis pelas preocupações relacionadas com este tipo de alimentação
Principais reações químicas com aditivos, conservantes e corantes:
Reação do ácido sórbico (C₆H₈O₂): Também identificado por (E200) é um conservante alimentar, eficiente na inibição de mofos, bolores e leveduras.
O H⁺ libertado torna o meio das células mais ácido matando os fungos
C₆H₈O₂ ⇌ C₆H₇O₂⁻ + H⁺
Em excesso pode causar irritação gástrica , no entanto é seguro nas doses regulamentadas.
Propionato de cálcio (ou propanoato de cálcio) (Ca(C₂H₅COO)₂): Também conhecido por (E282) é usado no pão do hambúrguer também para eliminar fungos.
Ca(C₂H₅COO)₂ → Ca²⁺ + 2 C₂H₅COO⁻
Estudos sugerem possível associação com alterações metabólicas quando consumido em excesso.
Pode afetar microbiota intestinal quando ingerido em grandes quantidades.
Glutamato Monossódico (MSG)/(C₅H₈NO₄Na): Realçador de sabor, o glutamato dissocia-se e liga-se a recetores específicos da língua (o quinto sabor, o umami) e intensifica o sabor da carne. Nas embalagens conhecido por (E621)
C₅H₈NO₄Na → Na⁺ + C₅H₈NO₄⁻
NITRITOS: Presentes em carnes processadas com o objetivo de inibir o crescimento de bactérias perigosas
NO₂⁻ + amina → nitrosamina
Através do calor da grelha podem reagir com aminas da carne formando Nitrosaminas que podem ser carcinogénicas.
Em conclusão:
Apesar de existirem alguns aspetos menos positivos associados aos conservantes utilizados, estes encontram-se presentes em quantidades muito reduzidas, geralmente insuficientes para provocar efeitos negativos na saúde quando consumidos dentro de padrões alimentares equilibrados.

Mas, afinal, se não são os conservantes e os aditivos químicos os principais responsáveis pelos impactos na nossa saúde, então o que estará verdadeiramente na origem desses efeitos?

Na realidade, o principal problema associado às cadeias de fast-food não está nos conservantes ou nos aditivos químicos, mas sim noutros fatores nutricionais. Destacam-se, sobretudo, o elevado teor de açúcar - presente em bebidas e sobremesas geladas como no próprio pão dos hambúrgueres — e a formação de peróxidos lipídicos durante a fritura de gorduras, resultante da sua oxidação pelo oxigénio:
lipídio + O₂ → peróxido lipídico
Em suma pode afirmar-se que os aditivos químicos não são o principal problema.
As reações associadas a estes compostos são bem conhecidas e controladas. Além disso, são utilizados em quantidades muito reduzidas, o que faz com que qualquer potencial impacto a nível celular seja mínimo ou praticamente impercetível dentro de um consumo normal.
O verdadeiro risco do fast-food está relacionado com a elevada ingestão calórica, sendo grande parte dessas calorias provenientes de gorduras saturadas, que podem aumentar o stress oxidativo do organismo, de açúcares refinados, capazes de provocar picos significativos de insulina, e do excesso de sal.
Assim, não é "a química" em si que prejudica a saúde, mas sim um padrão alimentar repetitivo, desequilibrado e consumido em excesso.

Rodrigo Araújo
2 mar 26
Entre Ciência e Estética:
A Verdade Transformadora sobre as Unhas de Gel!!
💡 Já ouviste falar da química poderosa por trás das unhas de gel? À primeira vista, pode parecer apenas um gesto simples: uma camada brilhante, uma luz intensa e alguns segundos de espera. Mas, na realidade, nesse breve instante, milhões de moléculas entram em ação para criar unhas mais bonitas, resistentes e duradouras!
🔎 As unhas de gel são um exemplo prático da aplicação da Química de Polímeros – a área que estuda como pequenas moléculas se ligam para formar materiais maiores, mais resistentes e extremamente versáteis.
Processo:
1. O gel é composto por monômeros e oligómeros acrílicos.
Ambos contêm moléculas com dupla ligação C=C, que reagem na polimerização.
- Monómero: molécula pequena, forma as cadeias principais do polímero e garante resistência final.
- Oligómero: molécula média, já parcialmente formada, fornece viscosidade e consistência.
No gel, monômero constrói; oligómero dá forma e suporte à rede 3D.
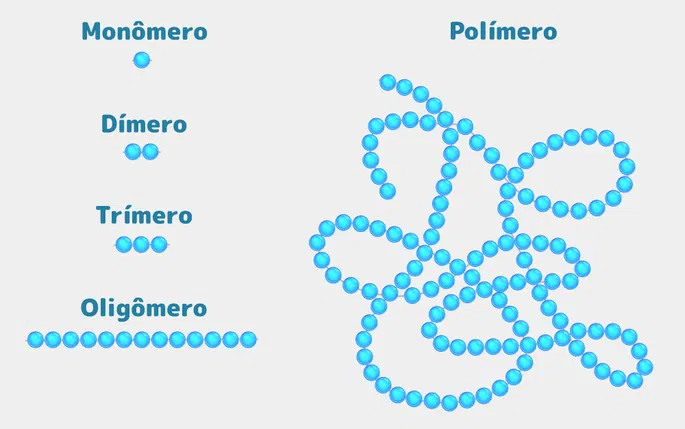
2. Quando o gel é exposto à luz UV (catalisador), os fotoiniciadores absorvem energia luminosa e formam radicais livres, que são moléculas ou átomos muito reativos com eletrão desemparelhado. Estes radicais iniciam a polimerização radicalar, que é a reação em cadeia na qual os monómeros se unem formando longas cadeias de polímeros.
3. Durante essa reação, forma-se uma rede tridimensional de polímeros, o que dá às unhas de gel características como dureza, resistência e durabilidade. Essa estrutura também permite que o gel mantenha a sua forma e não se dissolva facilmente em água.
4. O gel adere à unha natural principalmente através de aderência mecânica e interações químicas. Antes da aplicação, a superfície da unha é ligeiramente polida, criando pequenas irregularidades onde o gel consegue fixar-se. Além disso, existem forças intermoleculares entre o gel e a queratina, que é a proteína que constitui a unha natural.

------------------------------------------------------------------------------------------------------------------------------------
Em resumo, as unhas de gel nascem de uma reação química em que moléculas líquidas se unem sob a ação da luz UV ou LED, transformando-se em um polímero sólido que abraça a unha natural e oferece força, longa duração e um acabamento cheio de beleza e confiança. 🌺
Não é magia. É polimerização, ciência e beleza caminhando juntas! 🧪🧬
Cristiana Martins
23 fev 26

AirBags, como funcionam?
O sistema de funcionamento dos AirBags é constituído por uma resistência elétrica e por uma mistura de três substâncias: azida de sódio, nitrato de potássio e dióxido de silício. Quando ocorre a colisão, o sensor emite um impulso elétrico que faz a resistência do sistema aquecer-se a uma temperatura de 300°C. Isto provoca a decomposição da azida de sódio, produzindo sódio(Na) e nitrogénio(N), insuflando o AirBag.
2 NaN3 (s) → 2 Na (s) +3 N2 (g)
A Química pode acionar o airbag em milésimos de segundo, mas SÓ O CINTO DE SEGURANÇA SALVA A TUA VIDA! USA-O!
Vê o vídeo que demonstra como funcionam os AirBags
Diogo Silva
2 fev 26
A história de Marie Curie - Uma mulher radioativa!
Hoje, no Dia Internacional da Mulher, celebramos a vida e o legado de Marie Curie, uma pioneira na ciência que abriu caminho para muitas mulheres, desafiando barreiras de género numa época em que a ciência era dominada por homens.
Que a sua história inspire todas as mulheres a seguirem os seus sonhos, superando desafios e deixando a sua marca no mundo!
João Amorim, Luísa Meneses, Mara Costa, Maria Cunha e Nicole Matos
8 mar 25

Irmãs de Prometeu
A Química no Feminino
Na véspera da comemoração do Dia Internacional da Mulher, divulgo mais um livro de João Paulo André, editado em 2022, no qual é dado ênfase ao papel desempenhado pelas mulheres no campo científico.
Em Irmãs de Prometeu – A Química no Feminino, João Paulo André conta a história da ciência, centrada nas contribuições femininas para a ciência e em particular na química. Num período em que os homens dominavam a investigação científica, as mulheres tinham muitas dificuldades para mostrarem o seu valor, sendo muitas vezes (quase sempre) esquecidas e usurpadas. Neste livro ELAS são as protagonistas!
Como
curiosidade o título do livro compara as mulheres da química com Prometeu, um
titã que, segundo a mitologia grega, roubou o fogo a Héstia (Deusa grega) e deu-o aos Humanos (os mortais). Como castigo eterno, Zeus (Pai dos Deuses) mando-o ser acorrentado a uma rocha no Cáucaso onde o seu fígado era devorado todos os
dias por uma águia, apenas para vê-lo regenerar-se durante a noite,
segundo a lenda, devido à sua imortalidade.
Sobre o autor:
João Paulo André doutorou-se em Química na Universidade de Basileia e é Professor na Universidade do Minho.Tem mantido uma intensa atividade de divulgação da ciência.
Publicou vários artigos científicos e de divulgação, entre os quais uma análise da presença da química na obra de Eça de Queirós.
Possui dois livros editados, Poções e Paixões – Química e Ópera e mais recentemente Irmãs de Prometeu – A Química no Feminino.
José Armando Ferreira (prof.)
7 mar 25
O dia mais divertido do ano!
No dia 13 de dezembro voltou a realizar-se a atividade "Cientista por um dia".
O dia mais divertido do ano acontece no laboratório!
É uma atividade dinamizada pelo grupo disciplinar de Física e Química com a colaboração dos alunos de 11º e 12º anos, do Curso de Ciências e Tecnologias, direcionada para os alunos do 6ºano.
Olhares curiosos, sorrisos abertos e vontade de tocar, fazer, sentir!
E assim a Ciência acontece!
José Armando Ferreira (prof.)
19 dez 24
Como se transforma ar em pão?
O livro Como se transforma ar em pão? do famoso cientista português Nuno Maulide, revela-se uma verdadeira celebração da ciência ao alcance de todos. Professor de Química Orgânica na Universidade de Viena e reconhecido internacionalmente pelo seu trabalho, Maulide apresenta-nos uma obra que mistura ciência, curiosidade e simplicidade, despertando o interesse mesmo daqueles que não têm uma formação científica!
Seja para os curiosos que desejam aprender mais sobre o mundo que os rodeia, seja para os amantes da ciência que procuram uma leitura envolvente, Como se transforma ar em pão? é uma obra essencial. É mais do que um livro de ciência – é uma ponte para compreender a magia escondida nos processos do dia-a-dia e a importância do conhecimento científico na construção de um futuro mais sustentável e consciente.
Nicole Matos
06 dez 24
Vinagre:
O poderoso aliado natural na limpeza da tua casa
O vinagre é um ingrediente comum na cozinha, mas poucos sabem que ele pode ser um poderoso aliado na limpeza doméstica. Graças às suas propriedades ácidas e antibacterianas, o vinagre é capaz de eliminar sujidade, manchas e odores, oferecendo uma alternativa natural e económica aos produtos de limpeza tradicionais.

Reação com bicarbonato de sódio
Uma das reações mais populares de limpeza com vinagre é a neutralização do bicarbonato de sódio (NaHCO₃), que liberta dióxido de carbono (CO₂) e pode ajudar a desobstruir pias ou limpar superfícies.
NaHCO3 (aq) + CH3COOH (aq)→ NaCH3COO (aq) + H2O (l) + CO2 (g)
O que acontece:
Quando o vinagre (ácido acético) entra em contato com o bicarbonato de sódio, reage formando acetato de sódio (um sal), água e dióxido de carbono (que cria bolhas). Esse gás pode ajudar a soltar lixos e desobstruir pias ou ralos. Além disso, a reação gera efervescência, o que é útil para a limpeza de manchas ou resíduos difíceis.


Reação com depósitos de calcário
O vinagre é eficaz na dissolução de depósitos de calcário, como aqueles que encontramos em torneiras, chuveiros, máquinas de lavar e outros aparelhos. Isso ocorre porque o ácido acético reage com o carbonato de cálcio (CaCO₃) presente nesses depósitos.
CaCO3 (s) + 2 CH3COOH (aq)→ Ca(CH3COO)2 (aq) + H2O (l) + CO2 (g)
O que acontece:
O ácido acético (vinagre) reage com o carbonato de cálcio nos depósitos nas tubagens dos instrumentos e dissolve-o. Isso liberta dióxido de carbono (CO₂) na forma de bolhas e transforma o carbonato de cálcio em acetato de cálcio, uma substância mais solúvel em água.


Assim penso que podemos nomear o vinagre como "o super-herói da limpeza que não precisa de capa, só de garrafa" ou então "o vilão da sujidade e o herói da tua casa".

João Pedro Amorim
01 dez 24

Rómulo de Carvalho
Já ouviste falar de Rómulo de Carvalho? Não!? Tens a certeza?
Natural de Lisboa (1906-1997), foi professor de Ciências Físico- Químicas, um notável historiador da ciência, da pedagogia, um divulgador da cultura científica e, de um modo geral, da cultura Portuguesa.
Foi também poeta, conhecido pelo pseudónimo de António Gedeão, tendo publicado vários livros de poesia.
É autor de poemas conhecidos, como "Pedra Filosofal", "Calçada da Carriche" e "Lágrima de preta", entre outros.
Se queres conhecer mais a sua obra, clica aqui.
José Armando Ferreira (prof.)
28 nov 24
Porque é que choramos quando cortamos cebolas?
Decerto que se já cozinhaste ou viste alguém cozinhar e perguntaste "porque choramos quando cortamos cebolas?".
A explicação para este acontecimento é simples. Ao cortarmos uma cebola estamos a romper as suas células e estas libertam substâncias como óxidos sulfurados que sob o efeito de enzimas (alinases) transformam-se em ácidos sulfínicos, que como são muito voláteis, transforma-se em sin-propanetial-S-óxido.



Agora que sabemos o que a cebola liberta que nos fazer chorar, vamos perceber como é que efetivamente é provocada a reação de lacrimar.
Após a libertação do gás sin-propanetial-S-óxido no ar, este chega aos nossos olhos, e em contacto com a humidade neles presentes, ocorre a formação do ácido sulfúrico que provoca irritação nas terminações nervosas dos olhos. A reação ocorrida é traduzida pela equação química:
4 C3H6OS + 4 H2O → H2SO4 + 3 H2S + 4 C3H6O
Como resposta a esta reação o nosso cérebro estimula as glândulas lacrimais, que produzem lágrimas com a intenção de "limpar" os nossos olhos, reduzindo a irritação.


Mas existem maneiras de prevenir o choro, como por exemplo:
Luísa Meneses
18 nov 2024
Dos metais aos novos materiais:
o futuro é agora?
O avanço da ciência dos materiais tem desempenhado um papel fundamental na transformação da sociedade, desde as primeiras descobertas metalúrgicas até aos materiais altamente especializados que moldam o mundo moderno. Durante séculos, o uso de metais como o cobre, o bronze e o ferro impulsionou revoluções tecnológicas, levando a grandes saltos no desenvolvimento das civilizações. No entanto, estamos agora numa nova era, em que materiais inovadores, como compostos nanométricos, cerâmicas avançadas e polímeros de alta performance, começam a substituir o protagonismo dos metais. Faremos, então, uma viagem dos metais aos novos materiais, procurando responder à questão "o futuro é agora?".
A utilização dos metais ao longo a História
Clica aqui para teres acesso à evolução da descoberta dos metais nos vários períodos da história.
A utilização dos metais na atualidade
São poucos os metais que, no seu estado puro, servem para responder às necessidades do Homem, sendo assim, é necessário recorrermos às ligas metálicas.
As ligas metálicas são materiais obtidos através da junção de dois ou mais elementos químicos sendo que pelo menos um deles é um metal, sendo que este deve se encontrar em maior quantidade na mistura. As ligas metálicas são criadas com o objetivo de criar materiais com propriedades mais adaptadas às necessidades humanas e de reduzir os custos de produção.

A importância dos novos materiais
Cada vez mais se ouve falar em compósito, nanocompósitos e nanomateriais. O que são? Quais as suas aplicações?
Os compósitos são
materiais criados combinando dois ou mais materiais distintos para formar uma
nova substância. O compósito apresenta propriedades únicas e superiores às dos
materiais que o compõem. Partindo-se do exemplo de um compósito constituído por
dois materiais distintos, ambos mantém as suas propriedades individualmente,
mas, quando misturados, apresentam um comportamento muito distinto do
apresentado por ambos quando separados.

Os nanocompósitos são compósitos cujas partículas do reforço apresentam uma dimensão inferior a 100 nanómetros. O reduzido tamanho das partículas permite a otimização de inúmeras propriedades em relação aos materiais puros. Como exemplos de nanocompósitos podem citar-se o grafeno e as nanoargilas.

Os compósitos são conhecidos pela sua resistência, eficiência e durabilidade aprimoradas. Para além disso, apresentam um peso reduzido, o que lhes confere vantagem em relação aos metais comuns. Diferentes de muitos metais, os compósitos são altamente resistentes à corrosão e à ação de agentes químicos, o que aumenta sua durabilidade e reduz a necessidade de manutenção. As propriedades dos compósitos podem ser ajustadas de acordo com a necessidade da sua aplicação, permitindo a combinação de diferentes materiais (reforços e matrizes) para otimizar características como rigidez, resistência ao impacto, isolamento térmico e elétrico. Os compósitos são, dos novos materiais, aqueles que têm merecido maior investimento por parte da ciência e da tecnologia.
O grafeno é um material composto por uma camada única de átomos de carbono organizados numa estrutura hexagonal, semelhante a um favo de mel. É considerado um dos materiais mais promissores e revolucionários já descobertos, devido às suas propriedades físicas e químicas extraordinárias.

As principais características do grafeno incluem:
- Espessura de um átomo: O grafeno é extremamente fino, com apenas uma camada atómica de espessura, o que o torna o material bidimensional mais fino conhecido.
- Elevada condutividade elétrica e térmica: É um excelente condutor elétrico e térmico, permitindo a movimentação rápida de eletrões.
- Transparência: Apesar de ser composto por uma camada atómica de carbono, o grafeno é quase totalmente transparente, deixando passar cerca de 97% da luz branca.
- Extrema resistência: É cerca de 200 vezes mais resistente do que o aço, apesar da sua leveza, sendo um dos materiais mais fortes conhecidos.
- Flexibilidade: O grafeno pode ser dobrado ou deformado sem se partir, o que o torna ideal para aplicações em dispositivos flexíveis.
- Leveza: Embora seja extremamente forte, o grafeno é muito leve, uma característica importante para a sua utilização nas indústrias automóvel e aeroespacial, nomeadamente.

Os nanomateriais são materiais cujas estruturas externas, internas ou superficiais estão na escala nanométrica, que varia entre 1 e 100 nanómetros. Devido ao seu tamanho extremamente reduzido, apresentam propriedades físicas e químicas distintas em comparação com os materiais convencionais. Essas propriedades incluem uma maior área de superfície, o que pode resultar numa maior capacidade de acelerar reações químicas e melhor solubilidade.
Têm várias aplicações nas mais diversas indústrias, como sensores, diagnósticos médicos, tintas com proteção UV e enzimas artificiais. Outra aplicação popular de nanomateriais é nanotubos. Os nanotubos de carbono são um exemplo iluminativo do potencial da nanotecnologia e são também conhecidos por serem uns dos materiais mais fortes que foram produzidos pela nanotecnologia até os dias de hoje.

O futuro dos materiais revela-se já uma realidade indiscutível, impulsionado por avanços significativos desde os metais tradicionais até novos materiais como compósitos, nanotecnologias e materiais inteligentes. A inovação contínua neste campo está a moldar um futuro mais eficiente e tecnológico, mostrando que a era dos novos materiais não é apenas uma promessa, mas uma realidade presente. À medida que exploramos a fronteira entre a ciência e a tecnologia, percebemos que o futuro dos materiais está a concretizar-se rapidamente, moldando as mais diversas áreas, provando que "o futuro é agora".
João Amorim, Luísa Meneses, Mara Costa, Maria Cunha e Nicole Matos
18 out 24

Prémio Nobel da Química 2024
O Prémio Nobel da Química este ano foi atribuído aos cientistas David Baker (norte-americano) e Demis Hassabis e John Jumper (britânicos) pelos avanços tecnológicos na área das proteínas.
A Real Companhia de Ciências da Suécia premiou Baker pelo "Design da estrutura de proteínas" e Hassabis e Jumper por "previsões de estruturas de proteínas".
O Prémio Nobel da Química 2024 foi, assim, atribuído pelo estudo das proteínas, "as engenhosas ferramentas da vida".
Davis Baker conseguiu a proeza de construir tipos de proteínas totalmente novos, enquanto Demis Hassabis e John Jumper desenvolveram um modelo de IA (inteligência artificial) para resolver um problema de 50 anos: prever as estruturas complexas das proteínas.
Sobre os cientistas:
David Baker

David Baker é cientista da Universidade de Washington, Seattle, nos Estados Unidos. Conseguiu usar sequências de aminoácidos para criar novas proteínas únicas em 2003 e, "desde então, o seu grupo de investigação produziu proteínas criativas umas atrás das outras, incluindo proteínas que podem ser usadas como farmacêuticos, vacinas, nanomateriais ou microsensores".
Demis Hassabis (à esquerda) e John Jumper (à direira)

O trabalho de Demis Hassabis e John Jumper é mais recente, mas a sua base data dos anos 1970, quando se começou a tentar prever as estruturas das proteínas para aprender as suas aplicações. Estes cientistas fazem parte da Google DeepMind, um laboratório de inteligência artificial (que foi comprado pela Google em 2014) e que usa redes neuronais artificiais - desenvolvidas por John Hopfield, um dos vencedores do Nobel da Física anunciado na terça-feira - para várias outras aplicações, desde a biologia a videojogos.
José Armando Ferreira (prof)

A Química e a Arte
Será que a Química e a Arte são áreas que orbitam em planos diferentes?
A resposta mais óbvia a esta questão seria sim!
João Paulo André, no seu livro "Poções e Paixões - Química e Ópera" demostra que não! Ciência e Arte não só se tocam, como se fundem. Usando a Ópera como ponto de partida e pano de fundo (uma das suas paixões), o autor conduz-nos pelo mundo mágico das poções e das paixões, explicando-o através da Química.
Será que os voos das bruxas em vassouras, Harry Potter, a mãe do imperador Nero, a morte aparente de Julieta (da Peça de William Shakespeare ), a poção de amor de Tristão e Isolda (Ópera de Richard Wagner), têm algum algo em comum? A Química diz que sim!
Sobre o autor:
Publicou vários artigos científicos e de divulgação, entre os quais uma análise da presença da química na obra de Eça de Queirós.
José Armando Ferreira (prof.)
4 out 24

Quimiquices
Turma A do 12º Ano
Entra em contacto
Deixe um recado ou siga-me online
Será que tens curiosidade sobre o nosso trabalho ou tem sugestões para novos temas? Compartilha as tuas ideias ou as tuas sugestões.
